Carregando editor…
Previewdesktop · 720px
#65CN · NaturezaENEM - 2010 - 1° Dia
As misturas efervescentes, em pó ou em comprimidos, são comuns para a administração de vitamina C ou de medicamentos pra azia. Essa forma farmacêutica sólida foi desenvolvida para facilitar o transporte, aumentar a estabilidade de substâncias e, quando em solução, acelerar a absorção do fármaco pelo organismo.
As matérias-primas que atuam na efervescência são, em geral, o ácido tartárico ou o ácido cítrico que reagem com um sal de caráter básico, como o bicarbonato de sódio (NaHCO3), quando em contato com a água. A partir do contato da mistura efervescente com a água, ocorre uma série de reações químicas simultâneas: liberação de íons, formação de ácido e liberação do gás carbônico — gerando a efervescência.
As equações a seguir representam as etapas da reação da mistura efervescente na água, em que foram omitidos os estados de agregação dos reagentes, e H3A representa o ácido cítrico.
As matérias-primas que atuam na efervescência são, em geral, o ácido tartárico ou o ácido cítrico que reagem com um sal de caráter básico, como o bicarbonato de sódio (NaHCO3), quando em contato com a água. A partir do contato da mistura efervescente com a água, ocorre uma série de reações químicas simultâneas: liberação de íons, formação de ácido e liberação do gás carbônico — gerando a efervescência.
As equações a seguir representam as etapas da reação da mistura efervescente na água, em que foram omitidos os estados de agregação dos reagentes, e H3A representa o ácido cítrico.
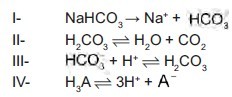
- AIV, I, II e III
- BI, IV, III e II
- CIV, III, I e II
- DI, IV, II e III.
- EIV, I, III e II
gabarito
Resolução
1° - IV - H3A ↔3H+ + A- essa equação apresenta a ionização do ácido cítrico, pois vemos que houve a separação das moléculas da substância de H3A em: 3H+ e A-.
2° - I - NaHCO3 →NA+ + HCO3 essa equação apresenta a dissociação iônica do bicarbonato de sódio, pois podemos observar a separação dos compostos formando um íon NA+ e o HCO3
3° - III - HCO3 + H+ ↔H2CO3 essa equação apresenta a formação do ácido carbônico.
4° - II - H2CO3 ↔H2O + CO2 essa equação apresenta a formação do gás carbônico