Carregando editor…
Previewdesktop · 720px
#81CN · NaturezaENEM - 2011 - 1° Dia
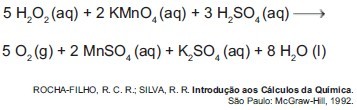
O peróxido de hidrogênio é comumente utilizado como antisséptico e alvejante. Também pode ser empregado em trabalhos de restauração de quadros enegrecidos e no clareamento de dentes. Na presença de soluções ácidas de oxidantes, como o permanganato de potássio, este óxido decompõe-se, conforme a equação a seguir:
- A2,0×100 mol.
- B2,0×10-3 mol.
- C8,0×10-1 mol.
- D8,0×10-4 mol.
gabarito - E5,0×10-3 mol.
Resolução
De início, é preciso calcular o número de mols de H2O2 em 20ml de uma solução, a qual a concentração é de 0,1mol/l por meio de uma regra de três simples:
0,1mol H2O2 -------------- 1000ml (1L)
X mol H2O2 ----------------20 ml
X=0,002 mol de H2O2
Ao analisar a questão, observa-se que para cada 5 mols de H2O2 faz-se necessário 2 mols de permanganato de potássio. Logo, aplica-se outra regra de três simples para encontrar a quantidade necessária de permanganato que irá reagir com com 0,002 mols de H2O2.
5 mols H2O2 ---------- 2mols KMnO4
0,002mols H2O2 ------------ X mols KMnO4
X=0,0008 ou 8,0×10-4 mol de KMnO4
Logo, a alternativa D está correta.