- Ametanol, pois sua combustão completa fornece aproximadamente 22,7 kJ de energia por litro de combustível queimado.
- Betanol, pois sua combustão completa fornece aproximadamente 29,7 kJ de energia por litro de combustível queimado.
- Cmetanol, pois sua combustão completa fornece aproximadamente 17,9 MJ de energia por litro de combustível queimado.
- Detanol, pois sua combustão completa fornece aproximadamente 23,5 MJ de energia por litro de combustível queimado.
gabarito - Eetanol, pois sua combustão completa fornece aproximadamente 33,7 MJ de energia por litro de combustível queimado.
Resolução
A Termoquímica estuda as quantidades de calor (energia) liberadas ou absorvidas, bem como as transformações físicas como a fusão, ebulição, condensação e outros, baseando-se nos princípios da termodinâmica.Sabendo-se desses conceitos da química, temos que essa questão trata-se desse assunto. Para resolver essa questão, teremos que calcular a energia liberada para cada litro de metanol e etanol queimado.
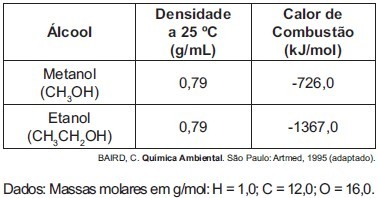
A densidade do metanol é igual a 0,79 g/ml, então 1L de metanol tem massa igual a 790 g.
1 mol de metanol tem massa igual a 32g. Logo, a quantidade de energia liberada pela queima de 1 litro de metanol é igual a:
32g.........................726 kJ
790g.........................X
X=17923 kJ ou 17,9 MJ
Para o etanol, temos:
1 mol de etanol tem massa igual a 46 g, então a quantidade de energia liberada na queima de 1 litro de etanol é igual a:
46g......................1367 kJ
790g...................Y
Y=23476 kJ ou 23,5 MJ
Utilizando o mesmo volume para os dois combustíveis, o etanol é mais vantajoso devido a sua combustão fornecer mais energia, aproximadamente 23,5 MJ por litro de combustível queimado. Portanto, a alternativa correta é a letra D.