Em uma aula prática de química orgânica, um professor identificou os frascos de várias substâncias apenas por suas fórmulas moleculares. Em seguida, apresentou a representação tridimensional da molécula do borneol, um álcool secundário, conforme a figura. Ele explicou que, quando oxidado, o borneol dá origem à cânfora, uma cetona usada desde a Antiguidade como incenso e no preparo de medicamentos. Finalmente, o professor solicitou que os alunos identificassem o frasco contendo a substância cânfora.
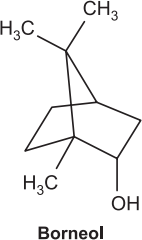
SANTOS, A. P. B. et al. Oxidação do borneol à cânfora com água sanitária: um experimento simples de baixo custo e limpo. Química Nova, n. 6, 2009 (adaptado).
O frasco contendo cânfora apresenta a fórmula molecular:
- A
C9H16O
- B
C9H17O
- C
C10H16O
gabarito - D
C10H16O2
- E
C10H18O2
Resolução
A questão aborda a oxidação do borneol, que é um álcool secundário, para formar cânfora, que é uma cetona. O borneol possui a fórmula molecular \(C_{10}H_{18}O\). Quando um álcool secundário é oxidado, ele perde dois átomos de hidrogênio: um do grupo hidroxila (-OH) e outro do carbono ao qual o grupo hidroxila está ligado. Isso resulta na formação de uma ligação dupla oxigênio-carbono, transformando o álcool em uma cetona.
No caso do borneol, a oxidação leva à formação da cânfora, que é uma cetona. A fórmula molecular da cânfora é \(C_{10}H_{16}O\). Isso ocorre porque, durante a oxidação, dois átomos de hidrogênio são removidos do borneol, resultando na perda de dois átomos de hidrogênio na fórmula molecular, mas o número de átomos de carbono e oxigênio permanece o mesmo.
Portanto, a fórmula molecular da cânfora, após a oxidação do borneol, é \(C_{10}H_{16}O\).