Um dos procedimentos mais rotineiros em análises químicas é a extração por solvente de materiais sólidos ou líquidos. No entanto, em pesquisas prospectivas, nas quais se pretende investigar a natureza química de determinado material, procede-se à extração por solventes em sequência, em ordem crescente de polaridade, conhecida como ordem eluotrópica. Em um processo de extração, foram utilizados os seguintes solventes:
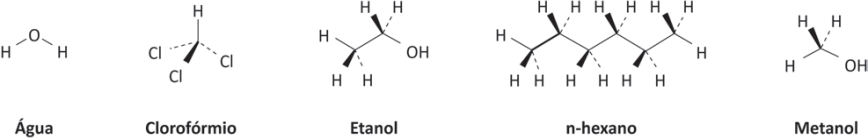
A sequência eluotrópica dos solventes utilizados é
- A
água, etanol, metanol, n-hexano e clorofórmio.
- B
etanol, metanol, água, clorofórmio e n-hexano.
- C
clorofórmio, n-hexano, metanol, etanol e água.
- D
n-hexano, clorofórmio, etanol, metanol e água.
gabarito - E
n-hexano, metanol, etanol, água e clorofórmio.
Resolução
Para determinar a sequência eluotrópica dos solventes, é necessário organizá-los em ordem crescente de polaridade. A polaridade de um solvente é influenciada pela sua estrutura molecular e pela presença de grupos funcionais polares.
1. n-Hexano: É um hidrocarboneto apolar, composto apenas por átomos de carbono e hidrogênio. Devido à sua estrutura linear e à ausência de grupos polares, é o solvente menos polar da lista.
2. Clorofórmio: Embora contenha átomos de cloro, que são eletronegativos, o clorofórmio é considerado pouco polar. Sua polaridade é maior que a do n-hexano, mas ainda é relativamente baixa.
3. Etanol: Possui um grupo hidroxila (-OH), que é polar, tornando o etanol mais polar que o clorofórmio. A presença do grupo hidroxila permite a formação de ligações de hidrogênio, aumentando sua polaridade.
4. Metanol: Semelhante ao etanol, mas com uma cadeia carbônica mais curta, o que aumenta a proporção do grupo polar na molécula. Isso faz com que o metanol seja mais polar que o etanol.
5. Água: É o solvente mais polar da lista. Sua estrutura molecular permite a formação extensiva de ligações de hidrogênio, conferindo-lhe uma polaridade muito alta.
Portanto, a sequência correta em ordem crescente de polaridade é: n-hexano, clorofórmio, etanol, metanol e água.