A penicilamina é um medicamento de uso oral utilizado no tratamento de várias doenças. Esse composto é excretado na urina, cujo pH se situa entre 5 e 7. A penicilamina, cuja fórmula estrutural plana está apresentada, possui três grupos funcionais que podem ser ionizados:
• carboxila: —COOH, cujo pKa é igual a 1,8;
• amino: —NH2, que pode ser convertido em amínio (—NH3+, cujo pKa é igual a 7,9);
• tiol: —SH, cujo pKa é igual a 10,5.
Sabe-se que pKa = -log Ka.
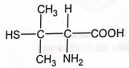
Penicilamina
Qual estrutura derivada da penicilamina é predominantemente encontrada na urina?
- A
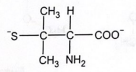
- B
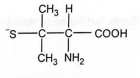
- C
gabarito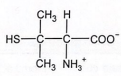
- D
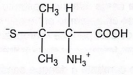
- E
Resolução
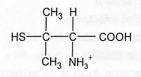
A resposta correta é a alternativa C, que mostra a estrutura da penicilamina com o grupo carboxila ionizado (-COO^-) e o grupo amino protonado (-NH3^+), enquanto o grupo tiol permanece não ionizado (-SH).
Para entender o porquê dessa ser a estrutura predominante na urina, precisamos considerar o pH da urina e os valores de pKa dos grupos funcionais da penicilamina.
O pH da urina varia entre 5 e 7. Quando o pH do meio é menor que o pKa de um ácido, o grupo funcional tende a permanecer na forma protonada (não ionizada). Quando o pH é maior que o pKa, o grupo tende a se ionizar.
Vamos analisar cada grupo funcional:
1. Carboxila: pKa = 1,8. Como o pH da urina (5 a 7) é maior que o pKa da carboxila, o grupo carboxila estará na forma ionizada (-COO^-).
2. Amino: pKa = 7,9. Como o pH da urina é menor que o pKa do grupo amino, ele estará na forma protonada (-NH3^+).
3. Tiol: pKa = 10,5. O pH da urina é muito menor que o pKa do tiol, então ele permanecerá na forma não ionizada (-SH).
Portanto, a estrutura predominante da penicilamina na urina terá o grupo carboxila ionizado e o grupo amino protonado, enquanto o grupo tiol permanecerá não ionizado, como mostrado na alternativa C.