Ao colocar um pouco de açúcar na água e mexer até a obtenção de uma só fase, prepara-se uma solução. O mesmo acontece ao se adicionar um pouquinho de sal à água e misturar bem. Uma substânci capaz de dissolver o soluto é denominada solvente; por exemplo, a água é um solvente para o açúcar, para o sal e para várias outras substâncias. A figura a seguir ilustra essa citação.
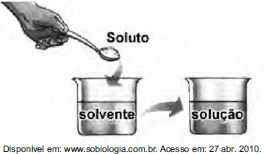
Suponha que uma pessoa, para adoçar seu cafezinho, tenha utilizado 3,42 g de sacarose (massa molar igual a 342 g/mol) para uma xícara de 50 ml do líquido. Qual é a concentração final, em mol/l, de sacarose nesse cafezinho?
- A
0,02
- B
0,2
gabarito - C
2
- D
200
- E
2000
Resolução
Essa questão caracteriza o assunto químico sobre soluções. Para iniciar, deve-se calcular o número de mols presente em 3,42 g de sacarose.
n = 3,42/342
n = 0,01 mol
Agora, calcular a concentração em mol/L
Concentração em mol/L=0,01mol /0,05 litro(L)
Concentração em mol/L=0,2mol/L