A invenção do LED azui, que permite a geração de outras cores para compor a luz branca, permitiu a construção de lâmpadas energeticamente mais eficientes e mais duráveis do que as incandescentes e fluorescentes. Em um experimento de laboratório, pretende-se associar duas pilhas em série para acender um LED azul que requer 3,6 volts para o seu funcionamento. Considere as semirreações de redução e seus respectivos potenciais mostrados no quadro.

Qual associação em série de pilhas fornece diferença de potencial, nas condições-padrão, suficiente para acender o LED azul?
- A
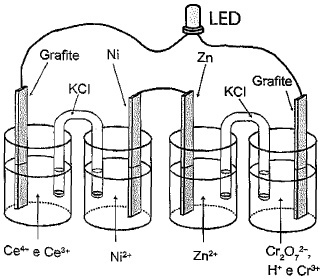
- B
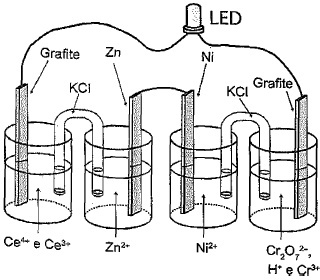
- C
gabarito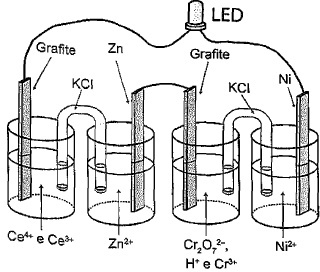
- D
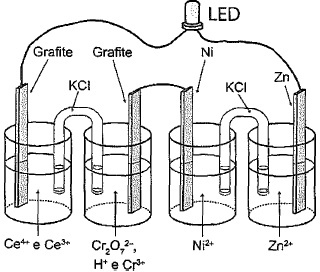
- E
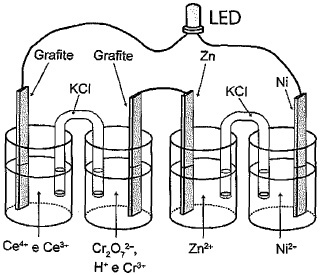
Resolução
O potencial gerado por pilhas conectadas em série é igual à soma dos potenciais das pilhas individuais, desde que estas estejam conectadas de forma correta. O anodo de uma pilha deve estar conetado ao anodo da outra. O anodo é o eletrodo no qual há oxidação (perda de elétrons). É o polo negativo da pilha. Os elétrons saem do ânodo (polo negativo) e entram no cátodo (polo positivo) da pilha.
As séries Ce-Zn + Cr2O7-Ni e Ce-Cr2O7 + Ni-Zn, entre estas, a que produz o maior potencial é a primeira, cujas pilhas são do tipo Metal – Agente oxidante:
2 x (Ce4+ + é → Ce3+ Ered = +1,61 V)
Zn → Zn2+ + 2 é Eoxi = +0,76 V
Fazendo os cálculos:
2 Ce4+ Zn → 2 Ce3+ + Zn2+ ⧍E1 = E1 + E2 = 2,37 V
Cr2O72- + 14 H+ + 6 é → 2 Cr3+ + 7 H2O Ered = +1,33 V
3 x (Ni → Ni2+ + 2 é Eoxi = +0,25 V)
Cr2O72- + 14 H+ + 3 Ni → 2 Cr3+ + 3 Ni 2+ + 7 H2O ⧍E2 = Ered + Eoxi = +1,58 V
⧍Etotal = ⧍E1 + ⧍E2 = 3,95 V
O potencial desta série de pilhas é maior que 3,6 V e, portanto, suficiente para acender o LED azul.