A escolha de uma determinada substância para ser utilizada como combustível passa pela análise da poluição que ela causa ao ambiente e pela quantidade de energia liberada em sua combustão completa. O quadro apresenta a entalpia de combustão de algumas substâncias. As massas molares dos elementos H, C e O são, respectivamente, iguais a 1 g/mol, 12 g/mol e 16 g/mol.
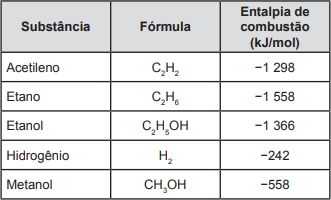
Levando-se em conta somente o aspecto energético, a substância mais eficiente para a obtenção de energia, na combustão de 1 kg de combustível, é o
- A
etano.
- B
etanol.
- C
metanol.
- D
acetileno.
- E
hidrogênio.
gabarito
Resolução
A resposta correta é o hidrogênio (H2) porque, entre as substâncias listadas, é a que libera a maior quantidade de energia por quilograma de combustível queimado.
Para determinar qual substância é a mais eficiente energeticamente, precisamos calcular a quantidade de energia liberada por quilograma de cada substância. Para isso, usamos a entalpia de combustão fornecida no quadro e as massas molares dos elementos envolvidos.
A entalpia de combustão é a quantidade de energia liberada quando um mol da substância é completamente queimada. A massa molar do hidrogênio é de 2 g/mol (considerando que a molécula de hidrogênio é diatômica, H2), então 1 kg de hidrogênio corresponde a 500 moles (1000 g / 2 g/mol).
A entalpia de combustão do hidrogênio é de -242 kJ/mol, o que significa que cada mol de hidrogênio libera 242 kJ de energia. Portanto, 1 kg de hidrogênio liberaria 242 kJ/mol * 500 moles = 121000 kJ.
Comparando com as outras substâncias, mesmo que algumas tenham entalpias de combustão mais altas por mol, suas massas molares são maiores, o que significa que menos moles de cada substância estariam presentes em 1 kg, resultando em menos energia total liberada por quilograma.
Portanto, o hidrogênio é a substância mais eficiente energeticamente para a obtenção de energia na combustão de 1 kg de combustível.