A eletrólise é um processo não espontâneo de grande importância para a indústria química. Uma de suas aplicações é a obtenção do gás cloro e do hidróxido de sódio, a partir de uma solução aquosa de cloreto de sódio. Nesse procedimento, utiliza-se uma célula eletroquímica, como ilustrado.
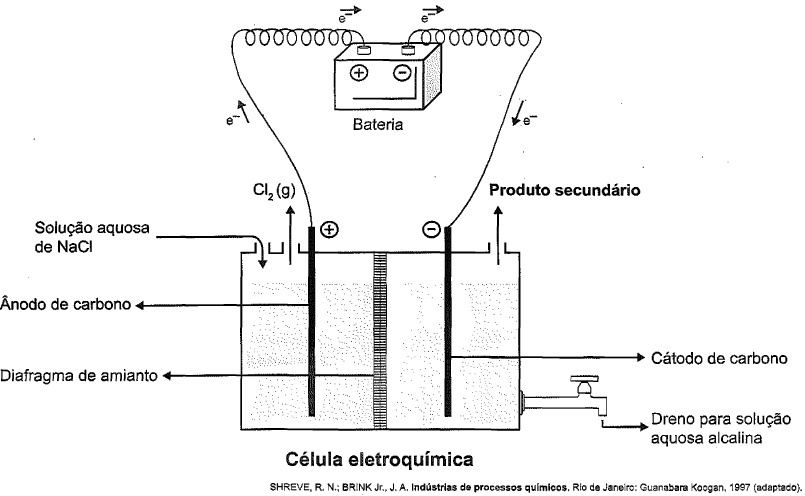
No processo eletrolítico ilustrado, o produto secundário obtido é o
- A
vapor de água.
- B
oxigênio molecular.
- C
hipoclorito de sódio.
- D
hidrogênio molecular.
gabarito - E
cloreto de hidrogênio.
Resolução
A resposta correta é a alternativa D) hidrogênio molecular.
Na eletrólise de uma solução aquosa de NaCl (cloreto de sódio), ocorrem reações de oxidação e redução nos eletrodos. No ânodo (eletrodo positivo), ocorre a oxidação dos íons cloreto (Cl-) presentes na solução, formando gás cloro (Cl2) e liberando elétrons:
\(2Cl^- \rightarrow Cl_2(g) + 2e^-\)
No cátodo (eletrodo negativo), ocorre a redução dos íons hidrogênio (H+) presentes na água, formando gás hidrogênio (H2) e consumindo elétrons:
\(2H^+ + 2e^- \rightarrow H_2(g)\)
Portanto, o produto secundário obtido no cátodo é o hidrogênio molecular (H2), que é liberado na forma de gás. As outras alternativas não são corretas porque o vapor de água (A) não é um produto da eletrólise, o oxigênio molecular (B) seria formado se a redução ocorresse nos íons oxigênio da água (o que não é o caso aqui), o hipoclorito de sódio (C) não é formado nesse processo e o cloreto de hidrogênio (E) também não é um produto da eletrólise de NaCl em solução aquosa.