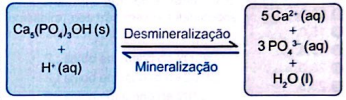
A hidroxiapatita, Ca5(PO4)3OH, é um mineral constituinte do esmalte dos dentes. Entre as diversas reações que ocorrem no meio bucal, encontram-se em equilíbrio as reações de desmineralização e mineralização da hidroxiapatita em meio aquoso, ilustradas a seguir. A desmineralização está associada à fragilização do esmalte do dente e à formação de cáries.
O uso de creme dental pode minimizar a perda da hidroxiapatita. O quadro apresenta o agente de polimento e o pH de alguns cremes dentais comerciais.
Creme dental | Agente de polimento | pH |
|---|---|---|
I | Bicarbonato de sódio | 9,5 |
II | Carbonato de cálcio | 11,0 |
III | Citrato de potássio | 7,7 |
IV | Dióxido de silício | 6,9 |
V | Fosfato de cálcio | 7,3 |
STORGATTO, G.A.; BRAIBANTE, M. E. F.: BRAIBANTE, H. A química na odontologia. Química Nova na Escola, V. 39, fev. 2017 (adaptado).
Considerando o equilíbrio químico envolvido, qual creme dental promove a maior desmineralização do esmalte do dente?
- A
I
- B
II
- C
III
- D
IV
gabarito - E
V
Resolução
A hidroxiapatita, \(\text{Ca}_5(\text{PO}_4)_3\text{OH}\), é um mineral essencial para a composição do esmalte dos dentes. O equilíbrio entre desmineralização e mineralização da hidroxiapatita é crucial para a manutenção da integridade do esmalte dental. A desmineralização ocorre quando a hidroxiapatita se dissolve em íons de cálcio (\(\text{Ca}^{2+}\)), fosfato (\(\text{PO}_4^{3-}\)) e hidróxido (\(\text{OH}^-\)) em meio aquoso, enquanto a mineralização é o processo inverso, onde esses íons se recombinam para formar a hidroxiapatita.
A desmineralização do esmalte está associada à fragilização do dente e à formação de cáries. O pH do meio bucal é um fator determinante nesse equilíbrio. Em ambientes mais ácidos (pH baixo), a desmineralização é favorecida, pois a concentração de íons \(\text{H}^+\) aumenta, deslocando o equilíbrio para a formação de íons solúveis. Em contrapartida, ambientes menos ácidos (pH mais alto) favorecem a mineralização, pois a concentração de íons \(\text{OH}^-\) é maior, promovendo a formação de hidroxiapatita.
Portanto, cremes dentais com pH mais baixo tendem a promover a desmineralização do esmalte, enquanto aqueles com pH mais alto ajudam a prevenir essa desmineralização. Analisando os pH dos cremes dentais apresentados, o creme dental com pH mais baixo (6,9) é o que mais favorece a desmineralização do esmalte, pois cria um ambiente mais ácido, deslocando o equilíbrio para a dissolução da hidroxiapatita.