O bisfenol-A é um composto que serve de matéria-prima para a fabricação de polímeros utilizados em embalagens plásticas de alimentos, em mamadeiras e no revestimento interno de latas. Esse composto está sendo banido em diversos países, incluindo o Brasil, principalmente por ser um mimetizador de estrógenos (hormônios) que, atuando como tal no organismo, pode causar infertilidade na vida adulta. O bisfenol-A (massa molar igual a 228 g/mol) é preparado pela condensação da propanona (massa molar igual a 58 g/mol) com fenol (massa molar igual a 94 g/mol), em meio ácido, conforme apresentado na equação química.
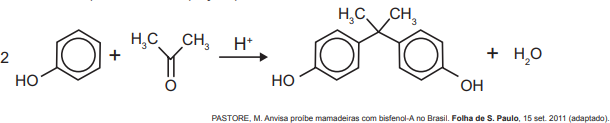
Considerando que, ao reagir 580 g de propanona com 3 760 g de fenol, obteve-se 1,14 kg de bisfenol-A, de acordo com a reação descrita, o rendimento real do processo foi de
- A
0,025%.
- B
0,05%.
- C
12,5%.
- D
25%.
- E
50%.
gabarito
Resolução
Para calcular o rendimento real do processo, primeiro precisamos determinar a quantidade teórica de bisfenol-A que poderia ser produzida com as quantidades dadas de reagentes.
A proporção estequiométrica entre propanona e fenol na reação é de 1:2, ou seja, para cada mol de propanona, são necessários 2 mols de fenol. A massa molar da propanona é 58 g/mol e a do fenol é 94 g/mol. Portanto, podemos calcular a quantidade de mols de cada reagente:
Mols de propanona = 580 g / 58 g/mol = 10 mols
Mols de fenol = 3760 g / 94 g/mol = 40 mols
Como a proporção é de 1:2, a quantidade limitante é a propanona, pois para 10 mols de propanona seriam necessários 20 mols de fenol, e temos 40 mols disponíveis. Portanto, a reação será limitada pela propanona.
Agora, vamos calcular a quantidade teórica de bisfenol-A que poderia ser produzida com 10 mols de propanona. A massa molar do bisfenol-A é 228 g/mol, então:
Quantidade teórica de bisfenol-A = 10 mols * 228 g/mol = 2280 g
O rendimento real do processo é a razão entre a quantidade real de bisfenol-A produzida e a quantidade teórica, multiplicada por 100 para obter a porcentagem:
Rendimento real = (quantidade real / quantidade teórica) * 100
Rendimento real = (1,14 kg / 2,28 kg) * 100
Rendimento real = (1140 g / 2280 g) * 100
Rendimento real = 0,5 * 100
Rendimento real = 50%
Portanto, o rendimento real do processo foi de 50%.