Um assistente de laboratório precisou descartar sete frascos contendo solução de nitrato de mercúrio(II) que não foram utilizados em uma aula prática. Cada frasco continha 5,25 g de Hg2(NO3)2 dissolvidos em água. Temendo a toxicidade do mercúrio e sabendo que o Hg2Cl2 tem solubilidade muito baixa, o assistente optou por retirar o mercúrio da solução por precipitação com cloreto de sódio (NaCl), conforme a equação química:
Hg2(NO3)2 (aq) + 2 NaCl (aq) → Hg2Cl2 (s) + 2 NaNO3 (aq)
Na dúvida sobre a massa de NaCl a ser utilizada, o assistente aumentou gradativamente a quantidade adicionada em cada frasco, como apresentado no quadro.
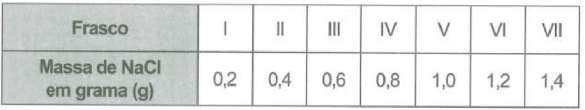
O produto obtido em cada experimento foi filtrado, secado e teve sua massa aferida. o assistente organizou os resultados na forma de um gráfico que correlaciona a massa de NaCI adicionada com a massa de Hg2Cl2 obtida em cada frasco. A massa molar do Hg2(NO3)2 é 525 g mol-1, a do NaCl é 58 g mol-1 e a do Hg2Cl2 é 472 g mol-1.
Qual foi o gráfico obtido pelo assistente de laboratório?
- A
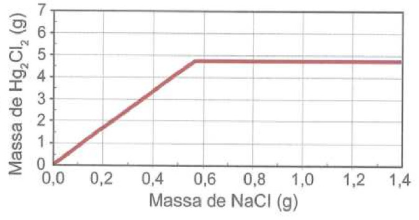
- B
gabarito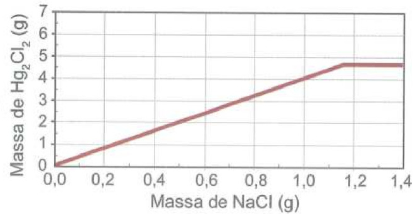
- C
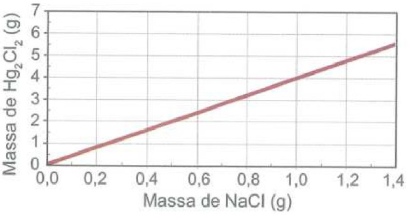
- D
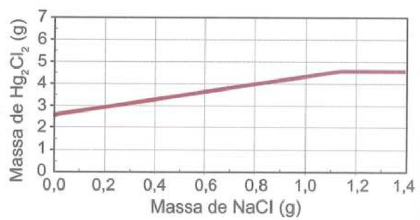
- E
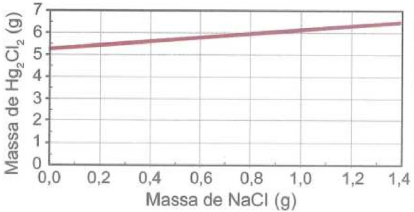
Resolução
A resposta correta é a alternativa B. Para entender o porquê, precisamos analisar a reação química e os dados fornecidos.
A reação química é:
\(Hg(NO_3)_2 (aq) + 2 NaCl (aq) \rightarrow HgCl_2 (s) + 2 NaNO_3 (aq)\)
A partir da equação, podemos ver que 1 mol de \(Hg(NO_3)_2\) reage com 2 mols de NaCl para formar 1 mol de \(HgCl_2\). A massa molar do \(Hg(NO_3)_2\) é 525 g/mol, a do NaCl é 58 g/mol e a do \(HgCl_2\) é 472 g/mol.
Cada frasco contém 5,25 g de \(Hg(NO_3)_2\), o que corresponde a 0,01 mol (5,25 g / 525 g/mol). Portanto, a quantidade estequiométrica de NaCl necessária para reagir completamente com o \(Hg(NO_3)_2\) em cada frasco é 0,02 mol (2 mols de NaCl para cada mol de \(Hg(NO_3)_2\)), ou seja, 1,16 g (0,02 mol * 58 g/mol).
O gráfico correto deve mostrar que, à medida que a massa de NaCl adicionada aumenta, a massa de \(HgCl_2\) obtida também aumenta, até atingir um ponto de saturação, onde a adição de mais NaCl não resulta em um aumento na massa de \(HgCl_2\) obtida. Isso ocorre porque todo o \(Hg(NO_3)_2\) disponível já reagiu, e o NaCl adicional não tem mais \(Hg(NO_3)_2\) para reagir.
A alternativa B mostra um gráfico com um aumento linear na massa de \(HgCl_2\) até cerca de 0,6 g de NaCl, que é aproximadamente a metade da quantidade estequiométrica necessária (1,16 g). Após esse ponto, a linha se torna horizontal, indicando que a adição de mais NaCl não está aumentando a massa de \(HgCl_2\) obtida, o que é consistente com a reação ter atingido seu limite estequiométrico.
As outras alternativas mostram gráficos que não correspondem ao comportamento esperado com base na estequiometria da reação e nas massas molares fornecidas.