Um sistema de pistão contendo um gás é mostrado na figura. Sobre a extremidade superior do êmbolo, que pode movimentar-se livremente sem atrito, encontra-se um objeto. Através de uma chapa de aquecimento é possível fornecer calor ao gás e, com auxílio de um manômetro, medir sua pressão. A partir de diferentes valores de calor fornecido, considerando o sistema como hermético, o objeto elevou-se em valores  como mostrado no gráfico. Foram estudadas, separadamente, quantidades equimolares de dois diferentes gases, denominados M e V.
como mostrado no gráfico. Foram estudadas, separadamente, quantidades equimolares de dois diferentes gases, denominados M e V.
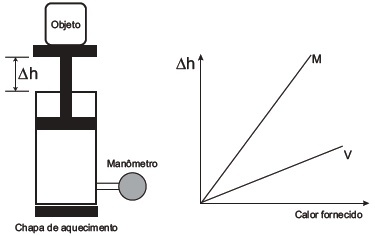
A diferença no comportamento dos gases no experimento decorre do fato de o gás M, em relação ao V, apresentar
- A
maior pressão de vapor.
- B
menor massa molecular.
- C
maior compressibilidade.
- D
menor energia de ativação.
- E
menor capacidade calorífica.
gabarito
Resolução
De acordo com a Equação de Clapeyron, temos:
p V = n R T
p A Δh = n R T
A pressão sobre o gás é mantida constante e, portanto:
\[\Delta h = \frac{nR}{pA}T\]Δh = kT
Para a mesma quantidade de calor fornecida, de acordo com o gráfico dado, o valor de Δh é maior para o gás M e, portanto, o gás M atingiu maior temperatura.
De acordo com a relação Q = C ΔT, em que C representa a capacidade calorífica do gás, concluímos que, para o mesmo Q, um valor maior de ΔT implica menor valor de C.
gás M: Δh maior ⇒ ΔT maior ⇒ C menor